I forbindelser kan fosfor optræde med alle formelle oxidationstrin mellem −3 og +5. Mest almindelige er oxidationstrinnene −3, +3 og +5.
Oxidationstrin −3. Mange metaller danner fosfider, hvor fosfor er i oxidationstrinnet −3, fx lithiumfosfid, Li3P. Fosfan, PH3, tidligere kaldt fosfin, er en farveløs, giftig luftart, der kan fremstilles ved reaktion mellem alkaliske vandige opløsninger og fosfider. Fosfans molekyle danner en tresidet pyramide med fosforatomet som pyramidespids. Heri ligner fosfan ammoniak, NH3, og arsan, AsH3, i overensstemmelse med, at nitrogen, arsen og fosfor står i samme gruppe i det periodiske system. I analogi med, at ammoniak danner ammoniumsalte, danner fosfan med syrer fosfoniumsalte, fx fosfoniumjodid, PH4I. Der kendes en række fosfor-hydrogenforbindelser med den generelle formel PnHn+2, fx difosfan, P2H4, hvor fosfor formelt har oxidationstrinnet −2. Også fosfaner med formel PnH3n+2 kendes, fx P4H14.
Oxidationstrin +3. Fosfor danner forbindelser af typen PX3, hvor X står for et af halogenerne fluor, klor, brom eller jod. Molekylformen er som fosfans, og forbindelserne er generelt reaktionsdygtige. Ved forbrænding af fosfor med begrænset tilførsel af oxygen dannes det giftige difosfortrioxid P2O3. Fosfonsyre med formel H3PO3, tidligere kaldt fosforsyrling, kan afledes af dette oxid; syren dannes også ud fra PX3 og vand ved reaktioner af typen 2 PX3 + 6 H2O ⇄ 2 H3PO3 + 6 HX. Konstitutionsformlen skrives som HPO(OH)2, idet et hydrogenatom er bundet til fosfor, og kun de to hydrogenatomer, der er bundet til oxygen, kan fraspaltes som hydrogenioner. Fosfonsyre anvendes som reduktionsmiddel.
Oxidationstrin +5. Halogenerne danner forbindelser af typen PX5. Ved reaktioner mellem PX3 og X2 indstiller der sig en ligevægt af typen PX3 + X2 ⇄ PX5. Ligevægten er mest forskudt mod højre for fluor og mindst for jod. Med vand kan disse forbindelser danne oxidhalogenider, fx fosfortrikloridoxid, POCl3. Brændes fosfor med rigelig tilførsel af luft eller oxygen, dannes difosforpentaoxid, P2O5, som er et snehvidt pulver. Krystallerne indeholder P4O10-molekyler. Opvarmes stoffet til 450 °C, omdannes det til en polymer form, hvor enkeltmolekyler ikke kan skelnes. Der findes også nogle fosforoxider, der formelt har oxidationstrin mellem +3 og +5, fx difosfortetraoxid, P2O4 (oxidationstrin +4). Strukturundersøgelser viser imidlertid, at stoffet indeholder lige dele af oxidationstrinnene +3 og +5. Difosforpentaoxid reagerer med vand og er det kraftigste kemiske tørringsmiddel, der kendes. Ved længere tids indvirkning af vand på difosforpentaoxid omdannes dette til fosforsyre, H3PO4, via en række mellemtrin. Fosforsyre kan fraspalte en, to eller tre hydrogenioner, H+, og danne henholdsvis dihydrogenfosfationer, H2PO4-, (mono)hydrogenfosfationer, HPO42-, og fosfationer, PO43-. Alle nævnte ioner danner salte med metalioner. Salte af mono- og dihydrogenfosfationer kaldtes tidligere fosforsure salte. Et af de vigtigste salte af fosfationen er calciumfosfat, Ca3(PO4)2, der dog ikke er stabilt i helt ren form. Som fosfat findes fosfor i naturen i store mængder som mineralet apatit, Ca5(PO4)3(OH,F), der ligesom calciumfosfat er tungtopløseligt, hvorfor disse salte ikke kan anvendes direkte som kunstgødning. Ved reaktion med svovlsyre danner de tungtopløselige fosfater det opløselige stof calciumdihydrogenfosfat, Ca(H2PO4)2, der er en vigtig bestanddel af kunstgødningen superfosfat.
Polyfosfater. Fosfationen, PO43-, er bygget som et tetraeder med fosfor i tetraederets tyngdepunkt og med oxygenatomerne i hjørnespidserne. Tetraedrene kan sættes sammen således, at et oxygenatom bliver fælles for to tetraedre. På den måde kan der dannes såvel kæder som ringe af tetraedre, dvs. polymere fosfater. I natriumtrifosfat, Na5P3O5, danner de tre fosfattetraedre en kæde.
Nitrogenforbindelser. Ved reaktion mellem fosforpentaklorid, PCl5, og ammoniumklorid, NH4Cl, ved ca. 140 °C dannes en række produkter kaldet fosfordikloridnitrid med sammensætning (PNCl2)n. I forbindelsen med n = 3 dannes en plan sekskant med skiftevis P- og N-atomer. De seks Cl-atomer er bundet til fosforatomerne; tre Cl-atomer ligger over P-N-planen, tre under. Ved videre opvarmning af fosfordikloridnitrid til ca. 300 °C dannes et gummiagtigt produkt med kædeformede molekyler.



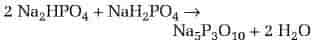

Kommentarer
Kommentarer til artiklen bliver synlige for alle. Undlad at skrive følsomme oplysninger, for eksempel sundhedsoplysninger. Fagansvarlig eller redaktør svarer, når de kan.
Du skal være logget ind for at kommentere.