Molekyle er den mindste enhed, som besidder alle egenskaber hos et stof. Et molekyle består af atomer, der holdes sammen af kemiske bindinger.
Faktaboks
- Etymologi
- Ordet molekyle kommer af fransk molécule, af nylatin molecula, dim. af moles 'masse'.

Molekyle. Figuren viser to molekyler, som begge har betydning for mennesker: Kolesterol er en vigtig bestanddel af blod, hvor indholdet af det bl.a. har betydning for åreforkalkning, og testosteron er det vigtigste mandlige kønshormon. Der er vist tre måder at anskueliggøre molekylsammensætning på. Den simpleste, men også den mindst informative angiver blot antallet af kulstof- (C), hydrogen- (H) og oxygenatomer (O). Den rumlige opbygning af molekylet kan illustreres ved hjælp af stregformler eller ved hjælp af den rumudfyldende model, hvor hvert atom er tildelt en størrelse svarende til dets atomradius. I stregformlerne udelades som oftest de atomare betegnelser på de atomer, som ikke har en særlig betydning for molekylets kemi. Fx angives kun OH-gruppen i kolesterol for at vise dets vigtigste egenskab, nemlig at dette molekyle er en alkohol. De forskellige måder at vise molekyler på har hver sin fordel. Fx kan man fra stregformlerne i figuren let se, at en stor del af testosteronmolekylet er identisk med ringdelen af kolesterol (den venstre del af dette molekyle). Dette fortæller, at de to molekyler er nært beslægtede. Den samme oplysning ses ikke så let i den rumudfyldte model.
Molekyle er den mindste enhed, som besidder alle egenskaber hos et stof. Et molekyle består af atomer, der holdes sammen af kemiske bindinger.
Begrebet molekyle fremkom i begyndelsen af 1800-tallet og tilskrives traditionelt fysikeren Amedeo Avogadro. Den fulde forståelse af årsagerne til molekyledannelse fik man dog først efter kvantemekanikkens fremkomst i 1920'erne. Det blev da muligt at forklare den systematik i molekyledannelsen, man havde kendt i temmelig mange år, fx at ædelgasserne kun vanskeligt indgår i molekyledannelse, og at der altid er fire bindinger til et kulstofatom i et molekyle.
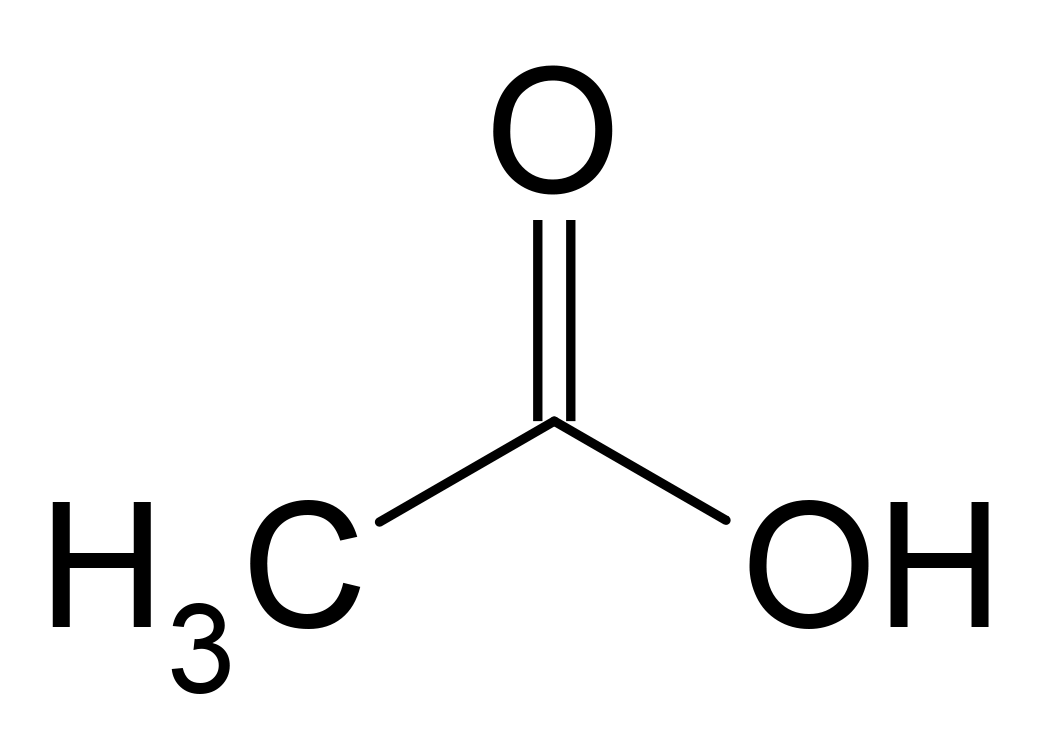
Et molekyle betegnes med en formel, som angiver, hvor mange atomer af hver slags der indgår i det, og hvorledes disse atomer er sammenbundet. Fx skrives formlen for eddikesyre CH3COOH (og ikke blot C2H4O2); denne formel fortæller, at eddikesyre består af carbon (C), hydrogen (H) og oxygen (O), og at atomerne er indbyrdes forbundet som angivet. Formlen angiver fx, at tre hydrogenatomer er bundet til carbon, og at et hydrogenatom er bundet til et oxygenatom. Det er sidstnævnte hydrogenatom, der er ansvarlig for syrevirkningen af eddikesyre.
Isolerede molekyler findes kun i gasfasen, dvs. for de fleste molekylers vedkommende ved lavt tryk og/eller høje temperaturer. Kun små, lette molekyler som fx kuldioxid (CO2) og methan (CH4) er gasformige ved normalt tryk og temperatur. Under påvirkning af intermolekylære kræfter, herunder hydrogenbindinger, dannes væsker og faste stoffer. I begge tilfælde kan både atomer og molekyler udgøre de elementære bestanddele. Faste stoffer opbygget af atomer holdes sammen af de noget stærkere kemiske bindinger.
Kendskab til atomernes indbyrdes placering i et molekyle er helt nødvendigt for at kunne forudsige dets egenskaber. Mange af kemiens nyere discipliner såsom krystallografi, molekylspektroskopi og kvantekemi har derfor som et af deres hovedformål at fastlægge geometrien af molekyler. Man undersøger, hvorledes atomerne er indbyrdes forbundet, og man måler afstande mellem dem (bindingslængder) og bindingsvinklerne i molekylet. Disse parametre angiver et molekyles konfiguration.
For visse meget usymmetriske (chirale) molekyler, fx CH3CHClBr, hvor et carbonatom er bundet til fire forskellige atomer eller grupper af atomer, er det også nødvendigt at kende deres absolutte konfiguration, dvs. hvorledes de adskiller sig fra deres spejlbilleder, for at kunne bestemme deres kemiske virkning. Stofomsætningen i mennesker og dyr kan ofte skelne mellem molekyler, som er hinandens spejlbilleder, såkaldte enantiomere forbindelser, og det er derfor vigtigt at kunne fastlægge et givet molekyles absolutte konfiguration for at kunne udtale sig om dets biologiske funktion.
Størrelsen af molekyler varierer inden for vide grænser. En typisk bindingsafstand mellem covalent eller ionisk bundne atomer er ca. 10-10 m, og det simpleste molekyle, H2 (dihydrogen), er således af denne størrelse. De største kendte molekyler indeholder millioner af atomer og har en udstrækning, som er tusinder af gange større. Det drejer sig bl.a. om makromolekyler som proteiner, nukleinsyrer og polymere forbindelser. Det er klart, at man ikke kan afbilde så store molekyler på den klassiske måde, dvs. med et atomtegn for hvert atom og med streger mellem disse til angivelse af bindingerne. Det er dog helt nødvendigt at have simple visualiseringer af molekyler for at kunne danne sig et overblik over deres funktioner, særligt inden for den molekylære biologi.
Nye molekyler fremstilles ved hjælp af kemisk syntese. Man kan fremstille molekyler med særlige egenskaber. Det kan være stoffer, som er efterspurgte i en eller anden anvendelsesmæssig sammenhæng, fx nye lægemidler, ukrudtsbekæmpelsesmidler eller plastmaterialer. Det er en proces, der ofte har mange komplicerede trin.
Man kan også fremstille biologisk aktive molekyler, fx molekyler med en given absolut konfiguration.
Den syntetiske kemi har udviklet sig med hastige skridt i slutningen af 1900-tallet, og man havde ved årtusindskiftet fremstillet og karakteriseret over 17 mio. forskellige kemiske forbindelser sammenlignet med skønsmæssigt ca. 1 mio., da udviklingen tog fart i 1960'erne, og vel omkring 100.000 ved år 1900. I 2015 havde man fundet eller fremstillet over 100 mio. kemiske forbindelser.
Kommentarer
Kommentarer til artiklen bliver synlige for alle. Undlad at skrive følsomme oplysninger, for eksempel sundhedsoplysninger. Fagansvarlig eller redaktør svarer, når de kan.
Du skal være logget ind for at kommentere.